Костный мозг – это губчатая мягкая ткань, содержащаяся внутри большинства костей человеческого скелета. Иногда его путают со спинным, однако эти ткани не имеют ничего общего между собой. Спинной мозг находится в позвоночнике и выполняет проводниковую и рефлекторную функции. Первая заключается в передаче нервных импульсов к головному мозгу и обратно, а вторая, как можно догадаться по ее названию, – в организации рефлексов. А вот какие особенности присущи костному мозгу, за что он отвечает и почему так важен для человека, сейчас разберемся.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.
Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — : крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Что собой представляет костный мозг?
Рисунок 1. Общая анатомия кости
[2]
Сочетание слов «костный» и «мозг» может сбивать с толку и навевать стереотипные образы. Под мозгом мы привыкли представлять «рыхлую массу» в форме грецкого ореха, располагающуюся в голове. Костный мозг интуитивно можем путать со спинным, ошибочно предполагая, что он располагается в позвоночном столбе.
На самом же деле, костный мозг (КМ) — это гемо- и лимфопоэтический орган, располагающийся в полостях губчатой части и костномозговых каналах костей (рис. 1).
Выделяют две разновидности КМ — красный, цвет которого обусловлен обилием крови и гемопоэтичеких клеток, и желтый, окраска которого связана с наличием большого количества жировых клеток (адипоцитов), замещающих большинство кроветворных клеток [1].
Первоначально у человека имеется только красная разновидность, которая по мере взросления частично переходит в желтую.
Красный костный мозг (рис. 2) состоит из ретикулярной стромы соединительной ткани, кровяных тяжей или островков клеток и синусоидальных капилляров. Строма представлена фибробластическими (стромальными = ретикулярными = адвентициальными) клетками, макрофагами и тонкими ретикулярными волокнами, состоящими из коллагена I типа, протеогликанов, фибронектинов и ламинина. Желтый костный мозг представляет собой подобную структуру, отличающуюся большим числом адипоцитов и меньшим количеством сосудов, гемопоэтических клеток [2].
Рисунок 2. Гистологический срез красного костного мозга. Т — трабекулы губчатой кости; А — адипоциты; S — синусоиды, заполненные кровью; C — кроветворные тяжи.
[1]
Кость представляет собой сложную материю, это сложный анизотропный неравномерный жизненный материал, обладающий упругими и вязкими свойствами, а также хорошей адаптивной функцией. Все превосходные свойства костей составляют неразрывное единство с их функциями.
Функции костей главным образом имеет две стороны: одна из них – это образование скелетной системы, используемой для поддержания тела человека и сохранения его нормальной формы, а также для защиты его внутренних органов. Скелет является частью тела, к которой крепятся мышцы и которая обеспечивает условия для их сокращения и движения тела. Скелет сам по себе выполняет адаптивную функцию путем последовательного изменения своей формы и структуры. Вторая сторона функции костей состоит в том, чтобы путем регулирования концентрации Ca2+ , H+ , HPO4+ в электролите крови поддерживать баланс минеральных веществ в теле человека, то есть функцию кроветворения, а также сохранения и обмена кальция и фосфора.
Форма и структура костей являются различными в зависимости от выполняемых ими функций. Разные части одной и той же кости вследствие своих функциональных различий имеют разную форму и структуру, например, диафиз бедренной кости и головка бедренной кости. Поэтому полное описание свойств, структуры и функций костного материала является важной и сложной задачей.
Структура костной ткани
«Ткань» представляет собой комбинированное образование, состоящее из особых однородных клеток и выполняющих определенную функцию. В костных тканях содержатся три компонента: клетки, волокна и костный матрикс. Ниже представлены характеристики каждого из них:
Клетки: В костных тканях существуют три вида клеток, это остеоциты, остеобласт и остеокласт. Эти три вида клеток взаимно превращаются и взаимно сочетаются друг с другом, поглощая старые кости и порождая новые кости.
Костные клетки находятся внутри костного матрикса, это основные клетки костей в нормальном состоянии, они имеют форму сплющенного эллипсоида. В костных тканях они обеспечивают обмен веществ для поддержания нормального состояния костей, а в особых условиях они могут превращаться в два других вида клеток.
Остеобласт имеет форму куба или карликового столбика, они представляют собой маленькие клеточные выступы, расположенные в довольно правильном порядке и имеют большое и круглое клеточное ядро. Они расположены в одном конце тела клетки, протоплазма имеет щелочные свойства, они могут образовывать межклеточное вещество из волокон и мукополисахаридных белков, а также из щелочной цитоплазмы. Это приводит к осаждению солей кальция в идее игловидных кристаллов, расположенных среди межклеточного вещества, которое затем окружается клетками остеобласта и постепенно превращается в остеобласт.
Остеокласт представляет собой многоядерные гигантские клетки, диаметр может достигать 30 – 100 µm, они чаще всего расположены на поверхности абсорбируемой костной ткани. Их цитоплазма имеет кислотный характер, внутри ее содержится кислотная фосфотаза, способная растворять костные неорганические соли и органические вещества, перенося или выбрасывая их в другие места, тем самым ослабляя или убирая костные ткани в данном месте.
Костный матрикс также называется межклеточным веществом, он содержит неорганические соли и органические вещества. Неорганические соли также называются неорганическими составными частями костей, их главным компонентом являются кристаллы гидроксильного апатита длиной около 20-40 nm и шириной около 3-6 nm. Они главным образом состоят из кальция, фосфорнокислых радикалов и гидроксильных групп, образующих [Ca10 (PO4) (OH)2], на поверхности которых находятся ионы Na+ , K+, Mg2+ и др. Неорганические соли составляют примерно65% от всего костного матрикса. Органические вещества в основном представлены мукополисахаридными белками, образующими коллагеновое волокно в кости. Кристаллы гидроксильного апатита располагаются рядами вдоль оси коллагеновых волокон. Коллагеновые волокна расположены неодинаково, в зависимости от неоднородного характера кости. В переплетающихся ретикулярных волокнах костей коллагеновые волокна связаны вместе, а в костях других типов они обычно расположены стройными рядами. Гидроксильный апатит соединяется вместе с коллагеновыми волокнами, что придает кости высокую прочность на сжатие.
Костные волокна в основном состоит из коллагенового волокна, поэтому оно называется костным коллагеновым волокном, пучки которого расположены послойно правильными рядами. Это волокно плотно соединено с неорганическими составными частями кости, образуя доскообразную структуру, поэтому оно называется костной пластинкой или ламеллярной костью. В одной и той же костной пластинке большая часть волокон расположена параллельно друг другу, а слои волокон в двух соседних пластинках переплетаются в одном направлении, и костные клетки зажаты между пластинками. Вследствие того, что костные пластинки расположены в разных направлениях, то костное вещество обладает довольно высокой прочностью и пластичностью, оно способно рационально воспринимать сжатие со всех направлений.
У взрослых людей костная ткань почти вся представлена в виде ламеллярной кости, и в зависимости от формы расположения костных пластинок и их пространственной структуры эта ткань подразделяется на плотную кость и губчатую кость. Плотная кость располагается на поверхностном слое ненормальной плоской кости и на диафизе длинной кости. Ее костное вещество плотное и прочное, а костные пластинки расположены в довольно правильном порядке и тесно соединены друг с другом, оставляя лишь небольшое пространство в некоторых местах для кровеносных сосудов и нервных каналов. Губчатая кость располагается в глубинной ее части, где пересекается множество трабекул, образуя сетку в виде пчелиных сот с разной величиной отверстий. Отверстия сот заполнены костным мозгом, кровеносными сосудами и нервами, а расположение трабекул совпадает с направлением силовых линий, поэтому хотя кость и рыхлая, но она в состоянии выдерживать довольно большую нагрузку. Кроме того, губчатая кость имеет огромную поверхностную площадь, поэтому она также называется Костю, имеющей форму морской губки. В качестве примера можно привести таз человека, средний объем которого составляет 40 см3 , а поверхность плотной кости в среднем составляет 80 см2 , тогда как поверхностная площадь губчатой кости достигает 1600 см2 .
Морфология кости
С точки зрения морфологии, размеры костей неодинаковы, их можно подразделить на длинные, короткие, плоские кости и кости неправильной формы. Длинные кости имеют форму трубки, средняя часть которых представляет собой диафиз, а оба конца – эпифиз. Эпифиз сравнительно толстый, имеет суставную поверхность, образованную вместе с соседними костями. Длинные кости главным образом располагаются на конечностях. Короткие кости имеют почти кубическую форму, чаще всего находятся в частях тела, испытывающих довольно значительное давление, и в то же время они должны быть подвижными, например, это кости запястья рук и кости предплюсны ног. Плоские кости имеют форму пластинок, они образуют стенки костных полостей и выполняют защитную роль для органов, находящихся внутри этих полостей, например, как кости черепа.
Кость состоит из костного вещества, костного мозга и надкостницы, а также имеет разветвленную сеть кровеносных сосудов и нервов, как показано на рисунке. Длинная бедренная кость состоит из диафиза и двух выпуклых эпифизарных концов. Поверхность каждого эпифизарного конца покрыта хрящом и образует гладкую суставную поверхность. Коэффициент трения в пространстве между хрящами в месте соединения сустава очень мал, он может быть ниже 0.0026. Это самый низкий известный показатель силы трения между твердыми телами, что позволяет хрящу и соседним костным тканям создать высокоэффективный сустав. Эпифизарная пластинка образована из кальцинированного хряща, соединенного с хрящом. Диафиз представляет собой полую кость, стенки которой образованы из плотной кости, которая является довольно толстой по всей ее длине и постепенно утончающейся к краям.
Костный мозг заполняет костномозговую полость и губчатую кость. У плода и у детей в костномозговой полости находится красный костный мозг, это важный орган кроветворения в человеческом организме. В зрелом возрасте мозг в костномозговой полости постепенно замещается жирами и образуется желтый костный мозг, который утрачивает способность к кроветворению, но в костном мозге по-прежнему имеется красный костный мозг, выполняющий эту функцию.
Надкостница представляет собой уплотненную соединительную ткань, тесно прилегающую к поверхности кости. Она содержит кровеносные сосуды и нервы, выполняющие питательную функцию. Внутри надкостницы находится большое количество остеобласта, обладающего высокой активностью, который в период роста и развития человека способен создавать кость и постепенно делать ее толще. Когда кость повреждается, остеобласт, находящийся в состоянии покоя внутри надкостницы, начинает активизироваться и превращается в костные клетки, что имеет важное значение для регенерации и восстановления кости.
Микроструктура кости
Костное вещество в диафизе большей частью представляет собой плотную кость, и лишь возле костномозговой полости имеется небольшое количество губчатой кости. В зависимости от расположения костных пластинок, плотная кость делится на три зоны, как показано на рисунке: кольцевидные пластинки, гаверсовы (Haversion) костные пластинки и межкостные пластинки.
Кольцевидные пластинки представляют собой пластинки, расположенные по окружности на внутренней и внешней стороне диафиза, и они подразделяются на внешние и внутренние кольцевидные пластинки. Внешние кольцевидные пластинки имеют от нескольких до более десятка слоев, они располагаются стройными рядами на внешней стороне диафиза, их поверхность покрыта надкостницей. Мелкие кровеносные сосуды в надкостнице пронизывают внешние кольцевидные пластинки и проникают вглубь костного вещества. Каналы для кровеносных сосудов, проходящие через внешние кольцевидные пластинки, называются фолькмановскими каналами (Volkmann’s Canal). Внутренние кольцевидные пластинки располагаются на поверхности костномозговой полости диафиза, они имеют небольшое количество слоев. Внутренние кольцевидные пластинки покрыты внутренней надкостницей, и через эти пластинки также проходят фолькмановские каналы, соединяющие мелкие кровеносные сосуды с сосудами костного мозга. Костные пластинки, концентрично расположенные между внутренними и внешними кольцевидными пластинками, называются гаверсовыми пластинками. Они имеют от нескольких до более десятка слоев, расположенных параллельно оси кости. В гаверсовых пластинках имеется один продольный маленький канал, называемый гаверсовым каналом, в котором находятся кровеносные сосуды, а также нервы и небольшое количество рыхлой соединительной ткани. Гаверсовы пластинки и гаверсовы каналы образуют гаверсову систему. Вследствие того, что в диафизе имеется большое число гаверсовых систем, эти системы называются остеонами (Osteon). Остеоны имеют цилиндрическую форму, их поверхность покрыта слоем цементина, в котором содержится большое количество неорганических составных частей кости, костного коллагенового волокна и крайне незначительное количество костного матрикса.
Межкостные пластинки представляют собой пластинки неправильной формы, расположенные между остеонами, в них нет гаверсовых каналов и кровеносных сосудов, они состоят из остаточных гаверсовых пластинок.
Внутрикостное кровообращение
В кости имеется система кровообращения, например, на рисунке показа модель кровообращения в плотной длинной кости. В диафизе есть главная питающая артерия и вены. В надкостнице нижней части кости имеется маленькое отверстие, через которое внутрь кости проходит питающая артерия. В костном мозге эта артерия разделяется на верхнюю и нижнюю ветви, каждая из которых в дальнейшем расходится на множество ответвлений, образующих на конечном участке капилляры, питающие ткани мозга и снабжающие питательными веществами плотную кость.
Кровеносные сосуды в конечной части эпифиза соединяются с питающей артерией, входящей в костномозговую полость эпифиза. Кровь в сосудах надкостницы поступает из нее наружу, средняя часть эпифиза в основном снабжается кровью из питающей артерии и лишь небольшое количество крови поступает в эпифиз из сосудов надкостницы. Если питающая артерия повреждается или перерезается при операции, то, возможно, что снабжение кровью эпифиза будет заменяться на питание из надкостницы, поскольку эти кровеносные сосуды взаимно связываются друг с другом при развитии плода.
Кровеносные сосуды в эпифизе проходят в него из боковых частей эпифизарной пластинки, развиваясь, превращаются в эпифизарные артерии, снабжающие кровью мозг эпифиза. Есть также большое количество ответвлений, снабжающих кровью хрящи вокруг эпифиза и его боковые части.
Верхняя часть кости представляет собой суставный хрящ, под которым находится эпифизарная артерия, а еще ниже ростовой хрящ, после чего имеются три вида кости: внутрихрящевая кость, костные пластинки и надкостница. Направление кровотока в этих трех видах кости неодинаково: во внутрихрящевой кости движение крови происходит вверх и наружу, в средней части диафиза сосуды имеют поперечное направление, а в нижней части диафиза сосуды направлены вниз и наружу. Поэтому кровеносные сосуды во всей плотной кости расположены в форме зонтика и расходятся лучеобразно.
Поскольку кровеносные сосуды в кости очень тонкие, и их невозможно наблюдать непосредственно, поэтому изучение динамики кровотока в них довольно затруднительно. В настоящее время с помощью радиоизотопов, внедряемых в кровеносные сосуды кости, судя по количеству их остатков и количеству выделяемого ими тепла в сопоставлении с пропорцией кровотока, можно измерить распределение температур в кости, чтобы определить состояние кровообращения.
В процессе лечения дегенеративно-дистрофических заболеваний суставов безоперационным методом в головке бедренной кости создается внутренняя электрохимическая среда, которая способствует восстановлению нарушенной микроциркуляции и активному удалению продуктов обмена разрушенных заболеванием тканей, стимулирует деление и дифференциацию костных клеток, постепенно замещающих дефект кости.
Какие функции выполняет кровеносная система?
Стабильное кровообращение необходимо каждому организму. Кровь выполняет множество разнообразных функций:
- Транспортная (связанная с переносом разнообразных веществ). Включает ряд частных функций, к которым относятся:
- дыхательная — перенос газов (кислорода и углекислого газа) как в растворенном, так и в химически связанном состоянии;
- трофическая — перенос питательных веществ из участков их всасывания и накопления к тканям;
- экскреторная — удаление из тканей продуктов метаболизма и их выделение из организма (с мочой, образующейся в почках в качестве фильтрата крови);
- регуляторная — перенос гормонов, факторов роста и других биологически активных веществ, осуществляющих регуляцию разнообразных функций, к клеткам разных тканей; распределение тепла между органами и его выделение во внешнюю среду (терморегуляторная функция).
- Гомеостатическая (связанная с поддержанием постоянства внутренней среды организма, в том числе кислотно-щелочного и осмотического равновесия, водного баланса, температуры тела, биохимического состава тканевых жидкостей и др.).
- Защитная (связанная с нейтрализацией чужеродных антигенов, обезвреживание микроорганизмов различными иммунными механизмами) [3].
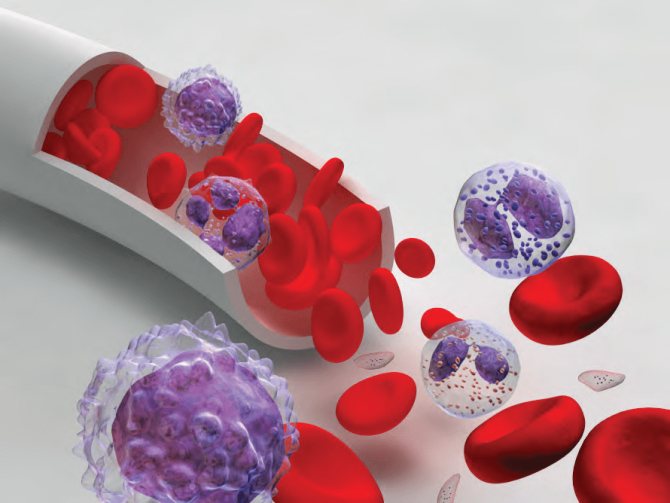
Столь большое разнообразие функций кровь может выполнять благодаря необычности своего гистологического строения: (1) форменные элементы (эритроциты, лейкоциты и тромбоциты) и (2) плазма (рис. 3). Источником форменных элементов является костный мозг. Бóльшая часть пула клеток формируется красным костным мозгом, остальная — желтым. [4].
Рисунок 3. Схема кровеносного сосуда с форменными элементами
[5]
Главные функции костного мозга
Первая и главная задача костного мозга – производство элементов крови, или гемопоэз. Поэтому нарушения в процессе кроветворения напрямую связаны с проблемами функционирования костного мозга. Если он не работает должным образом, возможно ухудшение самочувствия человека без, казалось бы, видимых на то причин.
Недостаточная активность костного мозга может вызывать такие состояния как:
- слабость и быстрая утомляемость (из-за нехватки гемоглобина, который отвечает за транспортировку кислорода);
- лихорадка (из-за недостаточного количества лейкоцитов);
- склонность к инфекционным заболеваниям (из-за снижения лейкоцитов, которые необходимы для борьбы с инфекциями);
- неровное дыхание (из-за нехватки эритроцитов и вызванным этим кислородным голоданием);
- кровоподтеки или кровотечения (из-за дефицита тромбоцитарной массы).
Кроме того, если вспомнить, что именно благодаря кровотоку все ткани и органы получают кислород и питательные вещества, то становится ясно: от костного мозга зависит абсолютно каждая клетка человеческого тела.
Также костный мозг – это стержневой элемент лимфатической системы. Все лимфоциты зарождаются именно в этой ткани. И если учесть, что иммунная система напрямую зависит от работоспособности лимфатической, то окажется, что без костного мозга не существовало бы и иммунитета. Большинство антител крови, которые защищают организм от патогенов, синтезируются именно в костном мозге.
Почему люди нуждаются в костном мозге?
Костный мозг является одним из центральных органов как кровеносной, так и иммунной систем [5]. Как отмечалось ранее, в нем находятся гемопоэтических стволовые клетки, способные дифференцироваться в различные клетки крови, например, в эритроциты, макрофаги или Т-лимфоциты.
Возникновение патологий этого органа приводит к снижению эффективности его деятельности, что ведет к ухудшению работоспособности иммунной и кровеносной систем. Организм человека становится более уязвимым. Возникает потребность в трансплантации донорского материала.
Нарушение целостности костного мозга может, произойти, например, при лечении онкозаболеваний. Вследствие применения химио- и лучевой терапии уничтожаются раковые, но вместе с ними и другие активно делящиеся клетки организма, в том числе, компоненты костного мозга. Организм теряет возможность производить форменные элементы крови.
Без трансплантации костного мозга подобное лечение нередко может принести больше вреда, нежели пользы, поскольку в итоге приводит к серьезным нарушениям в работе всего организма. В трансплантации нуждаются люди, больные лейкозом, апластической анемией, злокачественными лимфомами, аутоиммунными заболеваниями и пр.
За что отвечает красный костный мозг
Основной функцией, которую выполняет красный костный мозг, является функция кроветворения или гемопоэза. Она осуществляется постоянно и исключительно интенсивно – в кроветворных органах образуется более 300 млн. клеток крови в минуту. Функция кроветворения уникальна тем, что в нужное время и в нужном месте продуцируется огромное, но в то же время оптимальное количество клеток крови необходимого вида. Костный мозг может ускорить производство любой разновидности клеток крови в 5-6 раз, если организму требуется их больше. Все клетки крови развиваются из единой родоначальной клетки. Она имеет морфологию малого лимфоцита и называется мультипотентной гемопоэтической стволовой клеткой (ГСК). Ее потомками являются все клетки периферической крови. В процессе делений и дифференцировки мультипотентной ГСК образуется вся кроветворная ткань. Она объединяет как клетки-предшественники, так и созревающие и зрелые клетки крови: эритроциты, тромбоциты и лейкоциты, из которых состоит периферическая кровь человека.
Гемопоэз объединяет два больших отдела кроветворения: лимфопоэз и миелопоэз.
- Миелопоэз (или миелоидное кроветворение). В норме, единственным местом, где после рождения протекает данный процесс, является красный костный мозг. Там образуются все форменные элементы крови, кроме лимфоцитов (тромбоциты, эритроциты, моноциты и гранулоциты), чтобы затем поступить в периферическую кровь.
- Лимфопоэз (образование Т-лимфоцитов и В-лимфоцитов). После рождения реализуется в центральных и периферических лимфоидных органах. К первым относится красный костный мозг, а также тимус (который сохраняет функции лимфоидного органа лишь до половой зрелости организма); ко вторым – лимфатические узлы, селезенка и пейеровы бляшки ЖКТ.
Эритроциты, которые также называют «красные кровяные тельца» – клетки, не имеющие ядра, которым присуща форма двояковогнутого диска. Она поддерживается в эритроцитах благодаря спектрину (стабилизирующему белку мембраны). Размер эритроцита в норме колеблется между 7,5 мкм и 8,3 мкм, а продолжительность жизни составляет 90-120 дней. Всем известные основные группы крови (I, II, III, IV) выделяют на основании антигенных свойств эритроцитов. Функцию эритроциты выполняют чрезвычайно важную – они транспортируют дыхательные газы. Цитоплазма эритроцита заполнена гемоглобином на 96%. Это хромопротеид, состоящий из двух частей: глобина и гема. Первая является белковой, а вторая – небелковой и представляет собой комплекс протопорфирина IX и железа. Кислород из альвеол легких транспортируется к клеткам всего организма именно благодаря гемоглобину, и наоборот, от клеток к альвеолам – с помощью углекислого газа. В норме каждая молекула гемоглобина содержит две пары идентичных белковых цепей. Их обозначают буквами α и β из греческого алфавита. В зависимости от состава этих цепей различают три вида гемоглобина: эмбриональный, фетальный и гемоглобин взрослых.
В периферической крови помимо зрелых эритроцитов можно обнаружить молодые эритроциты – ретикулоциты. Это клетки без ядра, но содержат в себе большое количество РНК и рибосом, которые имеют мембранные рецепторы к трансферрину. РНК ретикулоцитов продолжает производить гемоглобин. На этой стадии возможна выработка гемоглобина до 30% от общего количества в эритроците. Большая же часть синтезируются на преретикулоцитных стадиях дифференцировки клетки – 70-80% гемоглобина. Когда ретикулоцит превращается в зрелый эритроцит, он больше не может производить гемоглобин, так как теряет РНК. В костном мозге эритроцит на стадии ретикулоцита находится в течение одного дня, а затем еще один день – в периферической крови.
Лейкоциты, названные, в свою очередь, белыми кровяными тельцами – это неоднородная (гетерогенная) группа клеток периферической крови, которые содержат ядро. Они выполняют функцию иммунитета и различаются по нескольким признакам. По форме ядра – сегментированное или округлое, по цвету и характеру цитоплазмы, а также по зернистости – ее наличию или отсутствию.
Если специфическая зернистость отсутствует, лейкоциты называются агранулоцитами, а если присутствует – гранулоцитами. К первым относятся лимфоциты и моноциты.
Гранулоциты же отличаются между собой характером специфической зернистости и бывают трех видов:
- Нейтрофилы (содержат обильную мелкую бледно-фиолетовую («нейтрофильную») зернистость).
- Базофилы (с крупной и необильной темно-фиолетовой («базофильной») зернистостью).
- Эозинофилы (отличаются зернистостью, занимающей всю цитоплазму клетки).
Благодаря лейкоцитам в организме реализуется защитная функция – иммунитет, который бывает специфический и неспецифический.
В одном из проявлений неспецифического иммунитета участвуют нейтрофилы, моноциты и тканевые макрофаги (в них превращаются моноциты после того, как выходят за пределы кровеносного русла). Они фагоцитируют (захватывают) с последующим лизисом (растворением) микробы, токсины и клеточный детрит (проще говоря, мусор). Эозинофилы обеспечивают защиту от паразитов и участвуют в аллергических реакциях (как и базофилы).
Лимфоциты осуществляют реакции специфического иммунитета, будь то врожденного или приобретенного. Специфический иммунитет, в свою очередь, бывает гуморальный и клеточный. Гуморальный иммунитет реализуется благодаря синтезу В-лимфоцитами иммуноглобулинов классов A, M, G, E, D; а клеточный – с помощью многообразных функций Т-лимфоцитов. Приобретенный иммунитет может формироваться естественным путем, вследствие различных инфекционных заболеваний, или в результате иммунизации организма.
Размеры лейкоцитов составляют от 6 мкм (малые лимфоциты) до 14 мкм (моноциты).
Лейкоциты отличаются между собой не только внешним видом и функцией, но и продолжительностью жизни. Так, например, длительность жизни лимфоцитов колеблется между несколькими часами и десятками лет. Моноциты циркулируют в крови на протяжении 72 часов, а потом выходят в ткани, где превращаются в фиксированные или мигрирующие макрофаги. Нейтрофилы находятся в крови 4-10 ч, с последующим выходом в ткани.
Тромбоциты – третий форменный элемент крови. Их приравнивают к истинным клеткам, хотя они и не являются таковыми. На самом деле, это частицы отшнуровавшейся цитоплазмы мегакариоцитов костного мозга, так называемые кровяные пластинки. Тромбоциты характеризуются свойствами агрегации (склеивания) и адгезии (прилипания). Их участие в механизмах свертывания крови и фибринолиза определяется наличием особых биологически активных веществ. Также они помогают поддерживать нормальную резистентность и функционирование микрососудов (ангиотрофическая функция). Размер тромбоцитов составляет 1-2 мкм, а продолжительность жизни – 8 суток.
Информированность о трансплантации костного мозга
Мы провели опрос группы потенциальных доноров (141 человека) из разных городов России (Санкт-Петербург, Москва, Орел, Казань и др.). Опросник состоял из 17 вопросов, 7 из которых были построены по методу семантического потенциала Ч. Осгуда.
В результате проведения опроса была установлена средняя осведомленность граждан по вопросу устройства костного мозга и его функций: более половины опрошенных (71%, то есть 100 человек) дали верное определение костному мозгу, из них наиболее полно и верно перечислили его функции 43% респондентов (рис. 4).
Рисунок 4. Диаграмма анализа информированности о костном мозге и его функциях
Большинство опрошенных (95,3%) знают о наличии донорства костного мозга в разной степени (от информированности о самом факте подобной операции, до сведений о многих деталях процесса). Люди осведомлены о проблеме благодаря СМИ (43,4% опрошенных), социальным сетям (50,4%) и близкому кругу (друзьям, родственникам) — 24%. Меньше половины респондентов задумывалось о том, что, став донором, смогли бы спасти жизнь (48,3%). Больше половины опрошенных (62,4%) (рис. 5) не стали бы совершать донацию костного мозга и не знают о наличии регистра доноров (65,4%). Респонденты в большинстве случаев не согласились бы сдавать костный мозг в связи со страхом получить болевые ощущения (47%) и необратимые травматичные изменения собственного здоровья (56,7%).
Рисунок 5. Диаграмма анализа количества потенциальных доноров костного мозга
Болезни костного мозга
Независимо от того, что вызвало повреждение ткани, особенно ее красной части – онкологическое заболевание или другие факторы – это всегда представляет угрозу для здоровья и жизни человека.
Миелопролиферативные расстройства
Нарушения со столь сложным названием возникают, если стволовые клетки размножаются неправильно. Таких заболеваний существует несколько типов:
- Первичный миелофиброз. Характеризуется образованием в костном мозге преимущественно мегакариоцитов и гранулоцитов. В финале болезни соединительная ткань разрастается, и кроветворение развивается вне костного мозга.
- Полицитемия. Это болезнь, характеризующаяся абсолютным повышением количества эритроцитов в периферической крови, повышением общего объема циркулирующей крови, нередко лейкоцитозом, гипертромбоцитозом, увеличением селезенки и частыми тромбозами мозговых и коронарных сосудов.
- Эссенциальная тромбоцитемия. Хроническое миелопролиферативное заболевание, проявляющееся гипертромбоцитозом (тромбоциты выше 450×109/л) в сочетании с мегакариоцитарной гиперплазией костного мозга, при отсутствии эритроцитоза, нейтрофильного лейкоцитоза.
Апластическая анемия
Апластическая анемия – это болезнь, из-за которой угнетается кроветворная функция костного мозга. Иными словами, он теряет способность производить необходимое для организма количество кровяных клеток. Такое случается из-за повреждения стволовых клеток, которые теряют способность расти и развиваться в новые клетки крови.
Апластическая анемия может быть приобретенной или врожденной. В первом случае стволовые клетки могут потерять способность превращаться в кровяные из-за воздействия токсинов, радиации или после тяжелых инфекционных заболеваний. Кроме того, эта болезнь иногда может проявляться как осложнение некоторых аутоиммунных нарушений, например, волчанки или ревматоидного артрита.
Лейкемия
Лейкемия, или “белокровие” – это вид рака, при котором в периферической крови появляется большое количество белых кровяных телец – лейкоцитов. Эти заболевания объединены под общим названием – гемобластозы.
Существуют такие принципы разделения гемобластозов:
- В зависимости от принадлежности к отделу кроветворения: к миелопоэзу относят миелопролиферативные новообразования, а к лимфопоэзу – лимфопролиферативные новообразования;
- В зависимости от места первичной локализации опухолевого роста: лейкозы (костный мозг) и гематосаркомы (вне костного мозга);
- В зависимости от агрессивности течения, коррелирующей с характером морфологического субстрата опухоли: из незрелых клеток (клеток-предшественников, бластов) либо из созревающих и зрелых клеток.
Ученым трудно сказать, что именно вызывает лейкоз. Но принято считать, что повышают риск онкологических процессов в костном мозге облучение, влияние некоторых химических веществ, а также ряд генетических болезней.
Трансплантация
Трансплантация КМ состоит из четырех этапов:
- предтрансплантационного (определения показаний к ТКМ; выбора донора; получения трансплантата; выбора и выполнения режима кондиционирования);
- собственно трансплантации (переливания гемопоэтических стволовых клеток);
- посттрансплантационного, включающего в себя сопроводительную терапию (асептический режим, медикаментозная профилактика, заместительная терапия, водно-электролитный баланс, венозный доступ); последний этап ТКМ — наблюдение за больным и контроль отдаленных результатов (летальный исход возможен в течение 100 дней) [6].
Трансплантация гемопоэтических клеток костного мозга бывает двух видов: аутологичная и аллогенная.
При аутологичной пересадке (рис. 6а) используются собственные стволовые клетки пациента. До жесткой химиотерапии отбираются и замораживаются клетки костного мозга. Далее, после проведения процедуры, они вводятся обратно в организм.
Аллогенная трансплантация (рис. 6б) представляет собой пересадку гемопоэтической ткани от здорового подходящего донора. Выделяют три вида подобной трансплантации (в зависимости от источника материала): совместимого родственного, совместимого неродственного и не полностью совместимого родственного происхождения.
Рисунок 6а. Схема аутологичной трансплантации костного мозга
НМХЦ им. Н.И. Пирогова
Рисунок 6б. Схема аллогенной трансплантации костного мозга
НМХЦ им. Н.И. Пирогова
Выделение нескольких типов обусловлено различием главного комплекса гистосовместимости (МНС) у разных людей и разной вероятностью возникновения осложнений при трансплантации.
Прежде чем обсудить непосредственно аллогенную трансплантацию, разберемся в том, что же такое МНС, откуда он берется и зачем нужен.
Главный комплекс гистосовместимости (МНС) — это несколько групп генов, кодирующих специфический мембранный белок — лейкоцитарный антиген человека (HLA), который осуществляет презентацию антигенов. Благодаря этому процессу происходит распознавание чужеродных антигенов и формирование адаптивного иммунного ответа. Основа последнего заключается в активации В-лимфоцитов, ответственных за формирование антител, и Т-лимфоцитов с макрофагами, обеспечивающих клеточный иммунитет (физическое удаление инородного агента). Поскольку комплекс гистосовместимости является тонкой структурой и направлен на защиту собственного организма, то у разных людей данный фактор может быть различен, следовательно, при смешивании биологических тканей, будь то кровь или костный мозг, есть шанс возникновения реакции «трансплантат против хозяина» (РТПХ). Проявление такой реакции может привести к полному неприживлению материала (иммунный ответ реципиента на клетки донора). Во избежание возникновения РТПХ до пересадки у донора и рецепиента определяют степень гистосовместимости путем HLA-типирования. По тому, насколько высока совместимость, и выделяют типы аллогенной трансплантации:
- Пересадка от совместимого родственного донора. При подобной донации материал является полностью совместимым по HLA-показателю и родственным пациенту. Донорами, как правило, являются братья и сестры больного.
- Пересадка от совместимого неродственного донора. Для данного типа трансплантации используется материал совместимый по лейкоцитарному антигену, но не родственный больному. Поиск доноров для этой трансплантации осуществляется через регистр. Данный путь является более длительным и дорогостоящим, нежели предыдущий (в связи с поиском, трансфером и обследованием донора), но может быть более эффективным, чем следующий тип.
- Пересадка от частично совместимого родственного донора. При проведении данной процедуры не требуется HLA-типирование, т.к. в роли донора выступает родитель, поскольку в таком случае донор является гаплоидентичным (совпадающим наполовину). Этот вид трансплантации применяется во врачебной практике недавно, поскольку ранее считалось невозможным избежать тяжелой РТПХ при неполной совместимости. Однако по данным многочисленных исследований [7], [8] установлено, что при неполной совместимости шансы избежать реакции «отторжения» такие же, как и при полной неродственной совместимости. Для проведения такой трансплантации используют дополнительные манипуляции с трансплантатом во избежание возникновение РТПХ, например, моделирование клеточного состава путем изменения направления поляризации лимфоцитов от Th1 к Th2 с помощью гранулоцитарного колониестимулирующего фактора (Г-КСФ).
Свято-Пантелеимоновский храм в станице Каневской
Идея единосущности, единородности, принципиальной близости мужчины и женщины – идея подлинно библейская. Женщина – не ущербная, а естественная, необходимая грань человеческого бытия; не восполнение какого-либо недостатка образа Божия в Адаме, а завершение его во всей полноте человеческого естества. При соединении в «одну плоть» зарождается новая человеческая личность.
После сотворения Адама Господь говорит, что быть человеку одному нехорошо. Удивительный контраст: всё было хорошо, и тем не менее, Адам не нашёл полноты жизни. Без жены, без верной спутницы, он оказался одиноким.
Поэтому в конце второй главы книги Бытия добавляются сведения о создании женщины: «И навёл Господь Бог на человека крепкий сон; и когда он уснул, взял одно из рёбр его, и закрыл то место плотию. И создал Господь Бог из ребра, взятого у человека, жену, и привёл её к человеку. И сказал человек: вот, это кость от костей моих и плоть от плоти моей; она будет называться женою, ибо взята от мужа» (Быт. 2, 12 – 23). Как понять это загадочное библейское изречение?
Интересно, что в рассказе о происхождении Евы используется глагол «бана» (построил, образовал), а не глагол «бара» (сотворил из ничего). Ева рождена от Адама, «взята от мужа» (Быт. 2, 23), «жена от мужа» (1 Кор. 11, 12). Но, несмотря на это, она всё-таки жена, а не дочь. В отличие от животных, она является помощницей и союзницей Адама в завете с Богом, полностью соответствующей своему супругу (Быт. 2, 18).
Теперь человек предстаёт в качестве двух отдельных и вполне самостоятельных лиц – мужа (иш) и жены (иша). Характерно, что на древнееврейском языке слова «жена», «женщина», производятся от слов «муж», «мужчина» путём прибавления родового окончания «а». Так же и в русском языке соотносятся слова «лис» и «лиса», «супруг» и «супруга».
Библия не уточняет сущность взятого из Адама. Еврейское слово «цела» переводится и как ребро, и как «грань», «сторона» (Исх. 25, 12 и 26, 20; 1 Цар. 6, 5 и 2, Цар. 16, 13). В данном контексте его нельзя рассматривать в анатомическом плане, ведь «кожаных одежд» Бог Адаму ещё не сделал (гл. V). «Всё это не следует, конечно, представлять в телесном виде, – подчёркивает блаженный Августин Иппонский, – подобно тому, что наблюдаем мы обычно у художников».
Язвительные выпады в адрес женщин, будто материалом для них послужила «безмозглая кость», по меньшей мере, нелепы. Кстати, ребро в своей полости имеет костный мозг. Достоинства Евы нисколько не умаляет и способ её создания. Как Ева рождена от Адама, так Христос – от Пресвятой Девы Марии (Лк. 1, 31 – 35), а Его Церковь (Невеста и Жена) – от Христа (Откр. 19, 7 и 22, 7).
Преподобный Ефрем Сирин делает Еве даже своего рода комплимент: «Ева была уже в Адаме… по телу… и по душе, и по духу; потому что Бог ничего не присовокупил ко взятой от Адама кости, кроме красоты и внешнего образа. Поскольку же в самой кости заключалось всё, что нужно было для образования из неё Евы, то справедливо сказано: «мужа и жену сотворил их».
«Ребро или кость здесь не есть что-то простое, – полагает святитель Иннокентий Херсонский. – Оно должно означать целую половину существа, отделившуюся от Адама во время сна. Как это происходило, Моисей не говорит, и это тайна. Ясно только, что прежде нужно было образоваться общему организму, который потом разделился на два вида – мужа и жену».
Творец выделил из Адама не какую-то часть костной системы, а ту сторону, в которой заключалась женская природа (гл. II). Ибо взять можно лишь то и лишь оттуда, что предварительно уже было, и было именно там. Господь разделил единое прежде на два пола, дабы потом, в Таинстве брака, снова объединить разделённое. Поскольку «Бог мужчину и женщину сотворил их», то «человек оставит отца своего и мать и прилепится к жене своей, и будут два одною плотью, так что они уже не двое, но одна плоть. Итак, что Бог сочетал, того человек да не разлучает» (Мк. 10, 6 – 9).
Отметим, что, изъяв у человека ребро, – самую близкую к сердцу кость – Бог прикрыл это место плотью. Здесь есть иносказание: обнажённое сердце мужчины покрывается плотью. Это знак того, что естественное влечение мужчины к женщине связано с плотским стремлением быть её мужем.
Увидев жену, Адам как бы от имени всех мужчин воспевает гимн любви: «Вот, это кость от костей моих и плоть от плоти моей; она будет называться женою»… Поистине, она – женская часть меня, я – мужская часть её. Так происходит в настоящем браке и доныне.
Столь уникальное единение возможно благодаря тому, что оба пола имеют единую природу. Действительно, кроме медико-психологических особенностей, у них нет существенной разницы. Главное биологическое и социальное отличие женщин и мужчин продиктовано детородными функциями. Вот почему достоинство полов перед Богом одинаково, и сочетаются они между собой как две части единого целого. Ни одна из этих частей не достигает совершенства без другой или без особого действия благодати Божией вне брака (например, в монашестве).
Идея единосущности, единородности, принципиальной близости мужчины и женщины – идея подлинно библейская. Женщина – не ущербная, а естественная, необходимая грань человеческого бытия; не восполнение какого-либо недостатка образа Божия в Адаме, а завершение его во всей полноте человеческого естества. При соединении в «одну плоть» зарождается новая человеческая личность.
Из книги «Что такое «наследственная порча»?».
Как происходит процедура типирования и донации стволовых клеток?
Для типирования и определения HLA-генотипа у потенциального донора берут образец крови до 10 мл [9]. Проводят лабораторные исследования и вносят полученную информацию в общероссийскую базу — Национальный регистр доноров.
Если потенциальный донор подходит больному, начинается процесс изъятия стволовых клеток. Его возможно осуществить двумя путями: шприцом из тазовой кости, или с помощью препаратов, которые способствуют выходу недифференцированных стволовых клеток в кровь. В первом случае, донора госпитализируют в больницу и под общим наркозом производят забор. В тазовой кости делают несколько маленьких разрезов, через которые специальными иглами извлекают около литра жидкого костного мозга (такой объем составляет не более 5% от общего количества и компенсируется организмом в течение двух недель).
Побочные эффекты для донора при данном способе забора могут быть следующими: болевые ощущения в тазовых костях, снижение уровня гемоглобина, тошнота, сонливость, слабость (последствия наркоза).
Во втором случае донор проходит подготовительный период (около пяти дней). В течение этого времени человеку подкожно вводится препарат (рекомбинантные факторы роста = гранулоцит-колониестимулирующий фактор = гранулоцит-макрофаг-колониестимулирующий фактор) для стимуляции пролиферации и мобилизации стволовых клеток. На пятый день донору проводят процедуру афереза (получение отдельных компонентов костного мозга путем центрифугирования) длительностью 3–5 часов. Кровь забирается из вены, проходит клеточный сепаратор (установку с несколькими камерами и системой подвода/вывода жидкости и клеточной культуры, предназначенную для разделения пула на группы по размеру, удельному весу и другим характеристикам) и возвращается донору. После прохождения через аппарат, из крови выделяют небольшое количество стволовых клеток. Процедура повторяется несколько раз для отбора необходимого количества материала. Суммарно через аппарат может проходить до 15 литров крови, из которых в сепараторе остается до 200 мл (остальное отправляется обратно донору).
Побочные эффекты для донора могут быть различны: ломота в костях, связанная с активным делением клеток костного мозга; обострение аутоиммунных заболеваний (например, артрита, красной волчанки).
Риски, связанные с серьезными последствиями для организма донора в обоих случая минимален, однако при применении перфузионного катетера есть шанс возникновения кровотечения, появления абсцесса или иной местной инфекции [6]. Как правило, спустя 2–3 недели все неприятные ощущения и последствия донации проходят.
В мировой практике существует регламент, по которому донор и реципиент не должны знать друг о друге. Максимум предоставляемой информации — возраст и пол. Знакомство может произойти лишь спустя два года после трансплантации. Донорам также не сообщают: помог ли их костный мозг вылечить больного. Это не тайна, а вынужденная анонимность. Регламент соблюдается в целях предосторожности и в силу психологических и этических причин.
Что это такое
Костный мозг
– важнейший орган, отвечающий за нормальную организацию системы кроветворения. В сферу его ответственности входит также обновление стволовых клеток и крови. Кровяные клетки, в процессе циркуляции по организму, периодически отмирают. Им на смену “приходят” новые клетки – те, которые образовались в костном мозге.
По своему внешнему виду орган является мягкой тканью, а если вы хотите узнать, где находится костный мозг у человека, то ответ будет – внутри костей. Отсюда происходит и его название.
Кроме того костный мозг содержит большое количество стволовых клеток – это незрелые клетки, по сути являющиеся эмбриональными. Именно стволовым клеткам дана удивительная возможность самовосстанавливаться и преобразовываться в клетки практически любого органа.
История от реального донора костного мозга
«Я заключила некую сделку с небесами», — говорит Алла Багирянц, которая стала реальным донором костного мозга. В 2015 году маме девушки поставили диагноз: множественная миелома (рак плазматических клеток крови). Это подвигло девушку изучить данную тему. Так она узнала, что при этом типе заболеваний может понадобиться пересадка костного мозга. Лечение миеломы проходило с помощью трансплантации аутологичных стволовых клеток. Это помогло матери Аллы, теперь она в ремиссии. Болезнь близкого человека послужила толчком, и девушка вступила в регистр доноров костного мозга в Центре гематологии.
В 2021 году Алла узнала, что есть совпадение со сторонним реципиентом и необходимо приехать в клинику для расширенного типирования. Следовало провести дополнительные анализы, чтобы удостовериться, что ни одно заболевание не осталось незамеченным. Пересаживать стволовые клетки от не совсем здорового человека может быть опасно для реципиента, ведь на момент трансплантации иммунитет пациента полностью подавлен.
«Когда наступил непосредственный момент донации, — говорит Алла, — меня проконсультировали о двух способах извлечения стволовых клеток: из тазобедренной кости и из периферической крови. Я выбрала второй вариант, доверясь врачам. Мне сделали укол лейкостима. Он стимулирует выход гемопоэтических клеток в кровь. Затем в обе руки вставили катетеры. Из одной забирали кровь, которая проходила через центрифугу, в которой сепарировались гемопоэтические клетки. А во вторую возвращали оставшуюся кровь, не содержащую стволовых клеток. По прошествии некоторого времени после начала донации у меня стали неметь конечности и лицо, но я быстро сообщила медсестрам, и они сделали мне укол, который помог. Весь процесс занял около четырех часов. После процедуры я чувствовала себя хорошо, единственной проблемой была небольшая ломота в костях. Стволовые клетки сдавала в два захода, так как с первого раза не получилось взять нужное количество. Вся донация не страшнее, чем обычная сдача крови».
Расширение базы регистра позволит быстрее находить «генетического близнеца» нуждающемуся, тем самым увеличивая его шанс на выздоровление.
Расположение и строение костного мозга
Располагается костный мозг внутри костей скелета, а именно в их пористой части (внутри полостей крупных трубчатых костей находится губчатая ткань). Кроме того, костный мозг расположен и в костях грудины, позвоночнике, ребрах, бедренных костях и костях черепа. Внутри позвоночника находятся стволовые клетки, благодаря которым происходят процессы генерации клеток крови, что крайне важно для жизнедеятельности организма. Около 50% от массы костного мозга составляет система кровеносных сосудов (синусоидов), диаметр которых варьируется в достаточно большом диапазоне. Стенки сосудов пористые, а поэтому вовнутрь них попадают необходимые элементы крови. Именно в сосудах происходит окончательное “созревание” кровяных клеток, после чего они проникают с током крови в вены самого костного мозга, а затем и в единую систему кровообращения организма.
Что происходит при трансплантации с больным?
Перед тем как приступить к введению гемопоэтических клеток, врачи проводят процедуру кондиционирования (химиотерапию или лучевую терапию). Это делается с целью уничтожения раковых клеток (если лечение касается онкозаболеваний) или подавления иммунной системы, чтобы увеличить шанс приживления донорских клеток. Такой процесс имеет свои негативные последствия: тошнота и рвота, выпадение волос, кровотечения, сердечная и почечная недостаточности.
Затем наступает следующий этап. После того как врачи сделали пункцию (прокол стенки сосуда, полости или какого-либо органа с лечебной или диагностической целью) у донора, начинается непосредственное переливание реципиенту. Стволовые клетки попадают в организм больного и начинают свою работу. Донорские клетки с течением времени компенсируют недостаток клеток костного мозга реципиента, налаживая кроветворение и иммунную систему. Процесс приживления обычно требует нескольких недель, после чего показатели крови начинают нормализовываться.
Риск развития патологических реакций существует на всех стадиях адаптации организма после трансплантации. Реакция может начаться в течение первых месяцев после пересадки или развиться куда позже. Это происходит вследствие того, что донорские клетки подвергаются иммунному ответу организма реципиента.
Клеточный состав
Наряду с вышеописанными основными компонентами, в костном мозге присутствуют также и другие его слагаемые: ретикулярные и остеогенные клетки, адипоциты, эндотелиоциты, макрофаги и межклеточное вещество. Ретикулярные клетки по форме напоминают объекты с отростками. Подобная форма обеспечивает возможность выполнения механической функции и секретирования таких слагаемых основного вещества, как проэластин, преколлаген, микрофибриллярный белок и др. Кроме того, ретикулярные клетки принимают активное участие в формировании достаточно специфичного кроветворного окружения, выделяя при этом ростовые факторы. Остеогенные клетки – это еще одна разновидность клеток костного мозга. Они также способны к выработке ростовых факторов и индуцированию гемопоэтических клеток. Самое активное кроветворение происходит в непосредственной близости от эндоста – соединительной ткани, которой выстлана внутренняя поверхность трубчатых костей. Именно здесь количество стволовых клеток наиболее высоко (концентрация больше в три раза в сравнении с центром полости).
Не менее постоянными слагаемыми костного мозга являются и жировые клетки (адипоциты). Примерно половина площади поверхности синусоидных капилляров покрыта адвентициальными клетками, способными к сокращениям под воздействием гемопоэтинов и некоторых других факторов. Их сокращение благоприятствует проникновению клеток в кровоток. Еще один элемент костного мозга – эндотелиальные клетки. Они активно участвуют в формировании стромы, процессах кроветворения, а также в синтезе коллагена 4-го типа и, конечно же, гемопоэтинов. Эндотелиальные клетки, из которых сформированы стенки синусоидов, вступают в непосредственный контакт со стромальными и гемопоэтическими клетками (это происходит благодаря прерывистости базальной мембраны). Помимо прочего, эндотелиоциты могут сокращаться, выталкивая кровяные клетки в капилляры, а затем закрывая поры, обеспечившие подачу новых клеток в кровоток. Эндотелиальные клетки продуцируют фибронектин, способствующий адгезии клеток друг к другу, и КСФ.
Имеются в костном мозге и макрофаги, которые представлены достаточно неоднородными клетками, имеющими различные свойства. Отдельные популяции макрофагов выделяют интерлейкины, эритропоэтин, интерферон, простагландины и др. Отростки макрофагов, проникая сквозь стенки капилляров, способны улавливать из кровотока трансферрин, после чего следует его подача к эритроцитам. Межклеточное вещество, как один из немаловажных компонентов костного мозга, имеет в своем составе коллаген трех типов, протеогликаны, гликопротеины и ряд других элементов.
Лечение спинного мозга с применением костного
Центральная нервная система имеет ограниченные способности к восстановлению, на которые негативно влияют различные факторы, в том числе связанные с повреждениями спинного мозга. Нарушения нервных структур и воспалительные процессы в них могут привести к инвалидности.
Однако исследования в области восстановления нейронов ЦНС дали почву для развития регенеративных методов лечения. Одним из многообещающих направлений в исследовании является метод введения стволовых клеток костного мозга совместно с плазмой крови, обогащенной тромбоцитами. Такой метод стимулирует регенерацию нейронов, поддерживая рост аксонов. Предполагалось, что данный вид лечения, с использованием концентрата клеток костного мозга, предпочтительнее из-за низкой способности на иммунный ответ и их большой распространенности.
На базе института Cedar Stem Cell Institute (штат Огайо, США) проводились процедуры ввода PRP (плазмы крови, обогащенной тромбоцитами) совместно с BMAC (концентратом стволовых клеток костного мозга) пациентам, имеющим повреждения в спинном мозге. Целью исследования было оценить изменения в состоянии пациентов, имеющих любой тип SCI (повреждение спинного мозга), а также отследить изменения индекса инвалидности ODI (показателя инвалидности, где более высокие значения эквивалентны более высокой инвалидности: от 0% до 100%).
Синонимы
Фразеологический оборот «до мозга костей» имеет целый ряд синонимов. Следует отметить, что в этом случае мы наблюдаем фразеологическое сращение слов, или другими словами – идиому. Здесь понимание целой фразы не складывается из значения отдельных слов.
Итак, приведем примеры синонимов для фразеологического оборота «до мозга костей»:
- с головы до ног;
- до кончиков ногтей;
- целиком и полностью;
- от кончика носа и до кончика хвоста;
- с головы до пяток;
- с макушки до пят.
Первый этап — выделение PRP и BMAC
Для получения PRP у пациентов отбирают по 60 мл периферической крови, добавляют 10 мл антикоагулянта цитратдекстрозы и центрифугируют полученную смесь с последующим концентрированием. В результате этого в среднем получается 7–8 мл плазмы, обогащенной тромбоцитами.
Получения BMAC проводят с помощью иглы для биопсии, которая через кожу и подкожные ткани вводится в правый гребень подвздошной кости. При помощи медленной аспирации отбирается 2 шприца по 25 мл, в которые добавляется по 1000 ед\мл гепарина. Полученную смесь фильтруют и центрифугируют в течение 10 минут, получая в итоге 17 мл BMAC.
После отбора PRP и BMAC смешивают в соотношении 1:2. Последним этапом данного метода является введение полученного препарата пациенту.
В эксперименте принимали участие семь человек с различными повреждениями спинного мозга, средний возраст пациентов составил 43,7 ± 2,33 года. После получения травмы пациенты перенесли минимум два вмешательства (физиотерапию и хирургическое вмешательство), а в период от 2,4 месяцев до 6,2 лет после травмы получили лечение смесью PRP и BMAC.
Показатели ODI отслеживали с помощью опроса по категориям: интенсивность боли, уход за собой, подъем, ходьба, положения сидя и стоя, сон, сексуальная жизнь, социальная жизнь и путешествия. Пациенты должны были оценить свое состояние от 0 (нет дискомфорта из-за травмы) до 5 (максимальный дискомфорт) в каждой категории. Все оценки складывались и делились на 50, чтобы получить процент функциональной инвалидности.
У 6 из 7 пациентов на момент начала эксперимента имелась значительная функциональная инвалидность. Один пациент после процедуры прекратил свои наблюдения, а динамика остальных пяти была отображена в исследовании. У двух пациентов наблюдались изменения от «тяжелой инвалидности» до «минимальной инвалидности», они вернули способность выполнять все бытовые дела самостоятельно. Показатели третьего пациента улучшились на 40% за год, а у четвертого улучшилось состояние на 28% за два месяца наблюдения.
Побочные эффекты наблюдались у одного из семи подопечных. Он не мог получать внутривенное введение препарата. Пациент сообщил о головной боли и трудностях, связанных с памятью.
Данный метод лечения помогает избежать дополнительного травмирования, которое возникает при введении инъекций в пораженный участок спинного мозга. Он безопасен и эффективен для восстановления после травм. У пациентов наблюдается положительная динамика и минимальное количество побочных эффектов. Потенциал такого лечения велик, и оно претендует занять передовое место при борьбе с повреждениями спинного мозга.
Функции ребер в организме человека
Фото: Depositphotos
Помимо вышеописанной задачи, ребра играют серьезную роль в защите жизненно важных внутренних органов человека от повреждений. Гибкий каркас предохраняет сердце и легкие от деформаций и ударов, не позволяет хозяину согнуться так, чтобы этим органам было трудно работать. Со стороны спины нижние ребра прикрывают печень и почки.
Природа наделила человека 12 парами ребер, которые состоят из той самой кости и хряща. Все они крепятся к спинным позвонкам при помощи суставов. Да, эти кости подвижны — это несложно заметить, наблюдая за дыханием человека. 7 верхних ребер примыкают к грудине и образуют грудную клетку.
Бывают случаи, когда от рождения у человека не хватает 1−2 нижних ребер или, наоборот, имеются лишние, чаще всего в области шеи. В редких случаях уникуму необходима операция. Чаще всего такой персонаж спокойно живет, не догадываясь о своих особенностях.
Может быть, медики древности были введены в заблуждение, относительно меньшего количества ребер у мужчины, получив образец вот такого необычного человека? Или им попалось женское тело с лишним ребром (подобная особенность чаще встречается у представительниц прекрасного пола)? В силу невозможности часто проводить вскрытия, они могли описать нестандартный вариант строения ребер, подтверждающий миф как норму.
Как сегодня ищут донора костного мозга?
Мировая практика показала, что данные о донорах, протипированных по HLA, лучше хранить в виде единой информационной базы. Регистр Всемирной ассоциации доноров костного мозга содержит данные 37 млн добровольцев из 55 стран.
Формирование РДКМ (регистр доноров костного мозга) в России только начинает набирать обороты. Например, Русфонд совместно с Первым Санкт-Петербургским государственным медицинским университетом им. академика Павлова создал базу доноров костного мозга. Регистр был назван в честь Васи Перевощикова — больного, умершего от лейкоза в девять лет из-за отсутствия донора. Сегодня в регистре числится 40 258 потенциальных доноров. Однако регистра, объединяющего все города России, — нет, что усложняет поиск донора по всей стране. База разрознена по городам и учреждениям, поэтому шанс встретить генетически подходящего донора составляет 1:10 000.
Обращение к зарубежным регистрам возможно не всегда, поскольку процедура донации от иностранного гражданина может стоить порядка 20–50 тысяч долларов. Помимо этого, из-за многовариантности генотипов (связанной, например, с многонациональностью России) поиски донора могут закончиться провалом, т.к. не будет обнаружен подходящий по HLA-типу человека.
Вследствие этого в 20–40% случаев поиск в европейских регистрах заканчивается неудачей.
«В России нет обобщенной базы доноров костного мозга, — комментирует Виктор Андронов, заслуженный донор России, основатель движения “Энергия жизни”. — Они сообщаются между собой, обмениваясь данными, но дружат не все. Проблема заключается в том, что у нас до сих пор отсутствует законодательная база — нет закона о донорстве костного мозга. Организация Русфонд создала большую базу доноров, которая сейчас является самой перспективной в стране.
Помимо отсутствия общероссийского регистра проблемой является недостаточная информированность людей. Многие путают костный со спинным мозгом, считают, что процедура является болезненной, а иногда и вовсе не знают о донорстве.
В идеале, в регистре должен быть каждый. Нам стоило бы жить под лозунгом: “Все помогают всем”. В условиях коронавируса это крайне важно, т.к. нам с иностранными донорами очень сложно в этот период.
Количество доноров в регистре — вопрос национальной безопасности и индекса человеческой отзывчивости».
Создание единого регистра является решением проблем с трансплантацией, поскольку это снизит затраты на поиск и активацию донора, что увеличит шансы на жизнь нуждающихся в пересадке.
Людей спасет отзывчивость и причастность к общему делу. Донорство способно объединять против общей проблемы, связанной с серьезными заболеваниями. Трансплантация костного мозга — шанс на жизнь.
Диагностика рака костного мозга в онкоцентре
Для того чтобы выявить рак костного мозга, требуется комплексный подход к обследованию. У человека производится сбор анамнеза и проводится физикальный осмотр. При этом специалист должен узнать обо всех жалобах и симптомах, которые ощущает сам пациент. Далее пациента направляют на обследование. Подозрения в наличие миеломы могут появиться после рентгенограммы костей. Лейкозы можно выявить, сделав общий анализ крови.
Подтверждение диагноза
Для того чтобы точно сказать о том, есть ли у человека онкология костного мозга, нужно провести морфологической исследование субстрата опухоли. Для этого пациент должен пройти пункцию или биопсию костного мозга.
Также специалисты онкоцентра проводят тесты, которые уточнят молекулярно-генетический профиль рака.
Все эти исследования необходимы для того, чтобы выбрать наиболее точную и наиболее действенную тактику лечения больного. Кроме того, данные анализов и тестов помогут выбрать оптимальный метод химиотерапии.
Литература
- Mescher A.L. Junqueira’s Basic Histology text and atlas. McGraw-Hill Education / Medical, 2021. — 576 p.;
- Sean J. Morrison, David T. Scadden. (2014). The bone marrow niche for haematopoietic stem cells. Nature
.
505, 327-334; - Быков В.Л. Цитология и общая гистология. Функциональная морфология клеток и тканей человека. СПб.: «Сотис», 2002;
- Шумаков В.И., Казаков Э.Н., Онищенко Н.А., Гуреев С.В., Остроумов Е.Н., Честухин В.В. и др. (2003). Первый опыт клинического применения аутологичныхмезенхимальных стволовых клеток костного мозга для восстановления сократительной функции миокарда. «Российский кардиологический журнал». 5, 42–50;
- What does my bone marrow do? (2016). Myelodysplastic Syndromes Foundation;
- Гедро Н.Н. (2013). Современное отделение трансплантации костного мозга. «Медицинская сестра». 2, 7–9;
- Субботина Н.Н., Долгополов И.С., Попа А.В., Бояршинов В.К., Пименов Р.И., Менткевич Г.Л. (2014). Гаплоидентичная трансплантация гемопоэтических стволовых клеток у детей с острыми миелоидными лейкозами: эволюция метода и собственные данные. «Клиническая онкогематология». 2, 131–136;
- O. V. Paina, N. V. Stancheva, Ye. V. Semenova, S. N. Bondarenko, O. A. Slesarchuk, et. al.. (2015). Haploidentical hematopoietic stem cell transplantation in the treatment of children and adolescents with resistant forms of acute leukemia. Ross. ž. det. gematol. onkol.
.
2, 39-45; - E. G. Khamaganova, L. A. Kuzmina. (2019). ASSESSMENT OF HLA-COMPATIBILITY AND REQUIREMENTS FOR HLA-TYPING OF PATIENT AND DONOR IN ALLOGENEIC HEMATOPOIETIC STEM CELL TRANSPLANTATION. Gematologiâ i transfuziologiâ
.
64, 175-187.